
(926)274-88-54
Бесплатная доставка.
Бесплатная сборка.
График работы:
Ежедневно. С 8-00 до 20-00.
Почта: soft_hous@mail.ru
 |
Звоните! (926)274-88-54 Бесплатная доставка. Бесплатная сборка. |
Ассортимент тканей График работы: Ежедневно. С 8-00 до 20-00. Почта: soft_hous@mail.ru |
|
Читальный зал --> Изменение энтропии Единицей измерения работы в СИ является джоуль (Дж). Отнеся работу расширения к 1 кг массы рабочего тела, получим l = L/M; Ы = Ы/М== = pdV/M = pd(V/M) = pdv. (2.5) Величина /, представляющая собой удельную работу, совершаемую системой, содержащей 1 кг газа, равна l=\pdi (2.6) Поскольку в общем случае р - величина переменная, то интегрирование возможно лишь тогда, когда известен закон изменения давления p = p(v). Формулы (2.3) - (2.6) справедливы только для равновесных процессов, при которых давление рабочего тела равно давлению окружающей среды. В термодинамике для исследования равновесных процессов широко используют р, у-диаграмму, в которой осью абсцисс служит удельный объем, а осью ординат - давление. Поскольку состояние термодинамической системы определяется двумя параметрами, то на р, у-ди-аграмме оно изображается точкой. На рис. 2.2 точка / соответствует начальному состоянию системы, точка 2 - конечному, а линия 12 - процессу расширения рабочего тела от v\ до V2- При бесконечно малом изменении объема dv площадь заштрихованной вертикальной полоски равна pdv~(>l\ 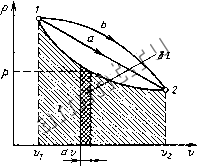 Рис. 2.2. Графическое изображение работы в р, и-координатах следовательно, работа процесса 12 изображается площадью, ограниченной кривой процесса, осью абсцисс и крайними ординатами. Таким образом,работа изменения объема эквивалентна плоиади под кривой процесса в диаграмме р, vj Каждому пути перехода системы из состояния / в состояние 2 (например, 12, 1а2 или 1Ь2) соответствует своя работа расширения: l\bi>l\a2>U2- Следовательно, \2абота зависит от характера термодинамического процесса! а не является функцией только исходного и конечного состояний системы. С другой стороны, \pdv зависит от пути интегрирования и, следовательно, элементарная работа б/ не является полным дифференциалом и не может быть представлена соотношением, аналогичным (2.1). Работа всегда связана с перемещением макроскопических тел в пространстве, например перемещением поршня, деформацией оболочки, поэтому она характеризует упорядоченную (макрофизи-ческую) форму передачи энергии от одного тела к другому и является мерой переданной энергии. Поскольку величина й/ пропорциональна увеличению объема, то в качестве рабочих тел, предназначенных для преобразования тепловой энергии в механическую, целесообразно выбирать такие, которые обладают способностью значительно увеличивать свой объем. Этим качеством обладают газы и пары жидкостей. Поэтому, например, на тепловых электрических станциях рабочим телом служат пары воды, а в двигателях внутреннего сгорания - газообразные продукты сгорания того или иного топлива. 2.3.ТЕПЛОТА Помимо макрофизической формы передачи энергии - работы существует также и микрофизическая, т. е. осуществляемая на молекулярном уровне форма обмена энергией между системой и окружающей средой. В этом случае энергия может быть передана системе без совершения работы.Мерой количества энергии, переданной микрофизическим путем, служит т е п л о т а J Теплота может передаваться либо при непосредственном контакте между телами (теплопроводностью, конвекцией), либо на расстоянии (излучением), причем во всех случаях этот процесс возможен только при наличии разности температур между телами. Как будет показано ниже, элементарное количество теплоты 6Q, так же как и 6L, не является полным дифференциалом в отличие от дифференциала внутренней энергии dU. За этой математической символикой скрыт глубокий физический смысл различия понятий внутренней энергии, теплоты и работы. Внутренняя энергия - это свойство самой системы, она характеризует состояние системы. Теплота и работа - это энергетические характеристики процессов механического и теплового взаимодействий системы с окружающей средой. Они характеризуют те количества энергии, которые переданы системе или отданы ею через ее границы в определенном процессе 2.4. АНАЛИТИЧЕСКОЕ ВЫРАЖЕНИЕ ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ Первый закон термодинамики представляет собой частный случай всеобщего закона сохранения и превращения энергии применительно к тепловым явлениям. В соответствии с уравнением Эйнштейна Е = тс надо рассматривать единый закон сохранения и превращения массы и энергии. Однако в технической термодинамике мы имеем дело со столь малыми скоростями объекта, что дефект массы равен нулю, и поэтому закон сохранения энергии можно рассматривать независимо. Закон сохранения и превращения энергии является фундаментальным законом природы, который получен на основе обобщения огромного количества экспериментальных данных и применим ко всем явлениям природы. Он утверждает, что энергия не исчезает и не возникает вновь, она лишь переходит из одной формы в другую, причем убыль энергии одного вида дает эквивалентное количество энергии другого вида. В числе первых ученых, утверждавших принцип сохранения материи и энергии, был наш соотечественник М. В. Ломоносов (1711-1765 гг.). Пусть некоторому рабочему телу с объемом V и массой М, имеющему температуру Т и давление р, сообщается извне бесконечно малое количество теплоты 6Q. В результате подвода теплоты тело нагревается на dT и увеличивается в объеме на dV. Повышение температуры тела свидетельствует об увеличении кинетической энергии его частиц. Увеличение объема тела приводит к изменению потенциальной энергии частиц. В результате внутренняя энергия тела увеличивается на dU. Поскольку рабочее тело окружено средой, которая оказывает на него давление, то при расширении оно производит механическую работу 6L против сил внешнего давления. Так как никаких других изменений в системе не происходит, то по закону сохранения энергии (>Q = dU + dL, (2.7) т. е. теплота, сообщаемая системе, идет на приращение ее внутренней энергии и на совершение внешней работы. Полученное уравнение является математическим вьЕражением первого закона термодинамики. Каждый из трех членов этого соотношения может быть положительным, отрицательным или равным нулю. Рассмотрим некоторые частные случаи. 1. 6Q = 0 - теплообмен системы с окружающей средой отсутствует, т. е. теплота к системе не подводится и от нее не отводится. Процесс без теплообмена называется адиабатным. Для него уравнение (2.7) принимает вид bL=-dU. (2.8) Следовательно, работа расширения, совершаемая системой в адиабатном процессе, равна уменьшению внутренней энергии данной системы. При адиабатном сжатии рабочего тела затрачиваемая извне работа целиком идет на увеличение внутренней энергии системьг 2. 6L = 0 - при этом объем телу не изменяется, dV = 0. Такой irponecc называется изохорным, для него 69 = dU, (2.9) т. е. количество теплоты, подведенное к системе при постоянном объеме, равно увеличению внутренней энергии данной системы. 3. dU = & - внутренняя энергия системы не изменяется и 6f = 6L, (2.19) т. е. сообщаемая системе теплота превращается в эквивалентную ей внешнюю работу. Для системы, содержащей I кг рабочего тела bq = du-\-bl. (2.11) Проинтегрировав уравнения (2.7) и (2.11) для некоторого процесса, получим выражение первого закона термодинамики в интегральной форме: Щ = U + Ц q = Au + l, (2.12) где hU -U2 - V1, Au = Ui - ui. 2.5. ТЕПЛвЕМКвСТЬ ГАЗ#В тношение количества теплоты 6, полученного телом при бесконечно малом изменении его состояния, к связанному с этим изменению температуры тела dT называется теплоемкостью тела в данном процессе: C = 6/dT. вбычно теплоемкость относят к единице количества вещества и в зависимости от выбранной единицы различают; удельную массовую теплоемкость с, отнесенную к 1 кг газа, Дж/(кг-К); удельную объемную теплоемкость с, отнесенную к количеству газа, содержащегося в 1 м объема при нормальных физических условиях, Дж/(м.К); удельную мольную теплоемкость р,с, отнесенную к одному ки-ломолю, Дж/(кмоль-К). Зависимость между удельными теп-лоемкостями устанавливается очевидными соотношениями; (2.13) Здесь р - плотность газа при нормальных условиях. Изменение температуры тела при одном и том же количестве сообщаемой теплоты зависит от характера происходящего при этом процесса, поэтому теплоемкость является функцией процесса. Это означает, что одно и то же рабочее тело в зависимости от процесса требует для своего нагревания на 1 К различного количества теплоты. Численно величина с изменяется в пределах от -(- оо до - оо. В термодинамических расчетах большое значение имеют: теплоемкость при постоянном давлении c = bq/dT, (2.14) равная отношению количества теплоты bqp, сообщенной телу в процессе при постоянном давлении, к измененинз температуры тела dT; теплоемкость при постоянном объеме cbqJdT, (2.15) равная отношению количества теплоты bq , подведенной к телу в процессе при постоянном объеме, к изменению температуры тела dT. В соответствии с первым законом термодинамики для закрытых систем, в которых протекают равновесные процессы, bq = du-\-pdv. С учетом соотношения (2.1) = {du/dT)dT + {{du/dv)r -h р] dv. (2.16) Для изохорного процесса (у == const) это уравнение принимает вид bq= = {duldT),dT, и, учитывая (2.15), получаем, что c = (du/dr) , (2.17) т. е. теплоемкость тела при постоянном объеме равна частной производной от его внутренней энергии по температуре и характеризует темп роста внутренней энергии в изохорном процессе с увеличением температуры. С учетом (2.2) для идеального газа c --=du/dT. (2.18) Для изобарного процесса (p==const) из уравнения (2.16) и (2.14) получаем с = {ди/дТ). +
ООО «Мягкий Дом» - это Отечественный производитель мебели. Наша профильная продукция - это диваны еврокнижка. Каждый диван можем изготовить в соответствии с Вашими пожеланияи (размер, ткань и материал). Осуществляем бесплатную доставку и сборку. Звоните! Ежедневно! (926)274-88-54 Продажа и изготовление мебели. Копирование контента сайта запрещено. Авторские права защищаются адвокатской коллегией г. Москвы. |